- Antecedentes de C-TAP[1]
El Fondo de Acceso Mancomunado a la Tecnología contra la COVID-19 (C-TAP, por sus siglas en inglés) de la Organización Mundial de la Salud (OMS) nació por la necesidad, de que en contexto de pandemia, existan mecanismos cuyo fin fuese la recopilación y puesta a disposición de datos y tecnologías para la fabricación a gran escala, tanto de medicamentos y vacunas como de otros productos eficaces para combatir la pandemia asegurando además su distribución rápida, equitativa y asequible a todos los países.
De esta manera, el 29 de mayo de 2020, la OMS junto al Medicines Patent Pool (MPP), la iniciativa Open COVID Pledge, y Unitaid, haciendo un llamado a la acción solidaria, lanzaron el Fondo de Acceso a la Tecnología COVID-19 (C-TAP) para facilitar el acceso oportuno, equitativo y asequible de los productos de salud COVID-19[2] promoviendo el intercambio de conocimientos, propiedad intelectual y know-how, mediante el uso de licencias no exclusivas sujetas o no a regalías.
- Finalidad de C-TAP
El C-TAP tiene por objeto servir de medio para acelerar el desarrollo de los productos necesarios para enfrentar la pandemia e impulsar la generalización de la producción y la eliminación de barreras de acceso, a fin de que pueda disponerse de los productos en todo el mundo. En otras palabras, C-TAP tiene como objetivos:
- Promover el desarrollo de la ciencia de forma abierta a fin de acelerar el desarrollo de productos compartiendo los derechos de propiedad intelectual, el know-how y los datos clínicos para facilitar la aprobación.
- Acelerar la fabricación a gran escala de los productos necesarios y facilitar el acceso equitativo de estas nuevas tecnologías a través de licencias transparentes, no-exclusivas y que cuenten con disposiciones en favor de la salud pública y la transferencia de tecnología.
- Promover el relacionamiento entre actores claves como financiadores, institutos de investigación, y gobiernos para que faciliten la transferencia de estas tecnologías y así maximizar el acceso a las mismas.
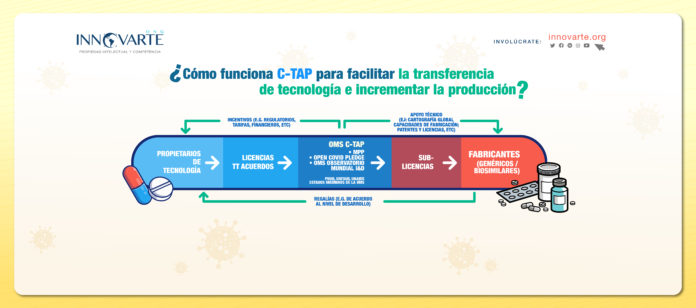
- Funcionamiento de C-TAP
El funcionamiento de C-TAP se basa en instituciones y plataformas existentes de forma previa que cooperan simultáneamente dentro de sus áreas para lograr la efectividad de este mecanismo, estas partes operacionales son:
1) La Alianza para el Acceso a la Tecnología (Tech Access Partnership)[3] , centrada especialmente en la promoción de la transferencia de tecnología y la producción local de equipos de protección personal (EPP), dispositivos médicos, como ventiladores y otras tecnologías relacionadas con el oxígeno, y materiales y componentes para el diagnóstico y realización de pruebas en los países de ingresos bajos y medianos. La Alianza para el Acceso a la Tecnología aprovecha los respectivos conocimientos especializados y mandatos de los organismos asociados para examinar exhaustivamente las transacciones de transferencia de tecnología entre los solicitantes de tecnología de los países de ingresos bajos y medianos y los titulares de tecnología de cualquier parte del mundo y formular recomendaciones al respecto. Los asociados llevan a cabo esas evaluaciones y ofrecen orientación en materia de procedimientos, en estrecha consulta con organizaciones e instituciones expertas en aspectos concretos de las tecnologías de interés, incluidos los contextos normativos, políticos, jurídicos y financieros en los que se llevarán a cabo las transacciones.
La Alianza para el Acceso a la Tecnología se centra actualmente en el apoyo a la transferencia de tecnología y la producción local de las tecnologías de lucha el COVID-19, con el fin de mitigar el impacto inmediato de la crisis y la consiguiente escasez en las cadenas de suministro, que afecta de manera desproporcionada a los países de ingresos bajos y medianos.
2) El Banco de Patentes de Medicamentos[4] amplió su mandato para incluir cualquier tecnología sanitaria que pudiera contribuir a la respuesta mundial al COVID-19. La experiencia con que cuenta el Banco de Patentes de Medicamentos en la facilitación del acceso a los medicamentos mediante su mecanismo de concesión voluntaria de licencias significa que podría desempeñar un papel fundamental al aplicar su experiencia en materia de propiedad intelectual y concesión de licencias sobre los productos y tecnologías patentados que se han señalado para la lucha contra el COVID-19, a fin de facilitar su disponibilidad a quienes más los necesitan. El Banco de Patentes de Medicamentos, a través de su base de datos MedsPaL de patentes y licencias en países de ingresos bajos y medianos, también está incorporando medicamentos candidatos que pueden ser adecuados para el tratamiento de las infecciones provocadas por el virus causante delCOVID-19.
3) Open COVID Pledge[5] : funciona actualmente como un repositorio de tecnologías principalmente materiales e inmateriales relacionadas con la COVID-19, pero está abierto a las ofertas de los fabricantes de vacunas o de tratamientos. Se trata de un mecanismo por el que las empresas ponen a disposición una licencia mundial no exclusiva, libre de regalías, por un periodo de tiempo limitado, hasta un año después de que la OMS declare finalizada la pandemia de COVID-19, o el 1 de enero de 2023, cualquiera que ocurra primero, salvo que el benefactor lo prorrogue. Hasta ahora, unas 30 empresas han anunciado sus compromisos, entre ellas grandes empresas de tecnología como Microsoft e IBM. En el Japón se ha puesto en marcha una iniciativa similar, denominada Open COVID-19 Declaration, que cuenta con el apoyo de 90 empresas y engloba cerca de un millón de patentes.
4) La Iniciativa mundial para intercambiar todos los datos sobre la gripe (GISAID) facilita un intercambio sin precedentes de datos genómicos y otros datos conexos sobre los casos de COVID-19, posibilitando así la epidemiología genómica y el progreso en tiempo real en el conocimiento de la nueva enfermedad y la investigación y el desarrollo de posibles medidas de respuesta médicas. Desde 2008, la GISAID ofrece a los Estados Miembros la posibilidad de elegir la forma de poner a disposición pública sus secuencias genómicas y los datos conexos sobre virus, de manera que ofrece transparencia en su utilización y constituye un mecanismo eficaz para salvaguardar los intereses de los participantes en sus datos . El acuerdo de licencia de acceso y utilización de datos de la GISAID se elaboró con la participación de los Estados Miembros. Si bien todos los datos son de acceso público, quienes comparten datos en el marco de la GISAID no pierden sus derechos inherentes sobre ellos . Los datos de la GISAID están abiertos a cualquiera, siempre y cuando se identifique el usuario, con el fin de fomentar la colaboración y permitir una supervisión eficaz para mantener los principios de intercambio establecidos. Un principio rector para quienes utilizan los datos en particular en una publicación es el requisito de reconocer la contribución del proveedor de los datos. En cambio, los archivos tradicionales de dominio público (por ejemplo, Genbank) solo ofrecen acceso y uso anónimos de los datos sin tener en cuenta los intereses de los proveedores de datos.
5) El Observatorio Mundial de la Investigación y el Desarrollo Sanitarios de la OMS es una «ventanilla única» exhaustiva y autorizada para obtener información y análisis actualizados sobre la investigación y el desarrollo sanitarios, que comprende recursos, procesos, productos y capacidad. Permite tomar decisiones fundamentadas en pruebas científicas en relación con las lagunas de investigación y desarrollo en materia sanitaria y con la financiación basada en las necesidades de salud pública. Esto se consigue mediante la consolidación, el seguimiento y el análisis de la información pertinente sobre la investigación y el desarrollo sanitarios, el aprovechamiento de los mecanismos de reunión de datos existentes y el apoyo a las acciones coordinadas de investigación y desarrollo sanitarios. El «Observatorio» abarca todas las esferas relacionadas con la salud y todos los tipos de investigación. Incluye datos y análisis sobre los productos sanitarios en curso, ensayos clínicos, inversiones en investigación y desarrollo y capacidad de investigación, entre otros. En respuesta a la pandemia de COVID-19, el Observatorio está reuniendo y actualizando continuamente una lista exhaustiva de sistemas de seguimiento y síntesis de datos sobre investigación y desarrollo en relación con la COVID-19 y elaborará análisis pertinentes y visualizaciones interactivas de datos de esos recursos, que incluirán los repositorios del C-TAP.
6) La base de datos del C-TAP de la OMS constituye el núcleo de las operaciones del C-TAP, ya que es el repositorio de los datos y los conocimientos técnicos sobre las tecnologías sanitarias fundamentales de la lucha contra la COVID-19 que formarán parte del C-TAP y de la formulación de los compromisos de los Estados Miembros en apoyo del C-TAP. La base de datos del C-TAP de la OMS actuará como plataforma de coordinación y estará conectada con otras plataformas de intercambio de datos y otras bases de datos en las que ya se dispone de información sobre la tecnología sanitaria relacionada con la COVID-19.
- Licencias celebradas por medio de C-TAP y MPP
A la fecha se están llevando a cabo conversaciones entre C-TAP y propietarios de tecnología vinculadas tanto al área de diagnóstico como al de vacunas, tratamientos, dispositivos médicos y plataformas digitales o software. Sin embargo, el mayor impacto se ha visto reflejado con compromisos de España y Estados Unidos.
1. España [6]
El 23 de noviembre de 2021 el C-TAP y el Banco de Patentes de Medicamentos (Medicines Patent Pool, MPP), ultimaron un acuerdo de licencia con el Consejo Superior de Investigaciones Superiores Cientificas (CSIC) de España en relación con una técnica de serología de anticuerpos contra el COVID-19. Con esta prueba se detecta eficazmente la presencia de anticuerpos anti-SARS-CoV-2 sintetizados en respuesta a la COVID-19 o a una vacuna.
La licencia apunta a facilitar la rápida fabricación y comercialización en todo el mundo de la prueba del CSIC para la detección serológica de la COVID-19. El acuerdo cubre el material biológico y todas las patentes conexas que hacen falta para fabricar la prueba. El CSIC proporcionará al MPP y los eventuales licenciatarios los conocimientos técnicos y la formación que se requieran. La licencia estará libre de regalías para los países de ingresos bajos y medianos y seguirá siendo válida hasta la fecha en que expire la última patente.
2. Estados Unidos[7]
El 12 de mayo de 2022 en la celebración de la segunda cumbre Global Covid-19 , copatrocinada por los Estados unidos, Belice, Alemania, Indonesia y Senegal, el gobierno de Estados Unidos, anunció el acuerdo de licencia entre C-TAP, Medicines Patent Pool y el Instituto Nacional de Salud (NIH) de los Estados Unidos para el desarrollo de varias terapias innovadoras, vacunas en etapa temprana y herramientas de diagnósticos para COVID-19.
Las licencias, que son transparentes, globales y no exclusivas, permitirán a los fabricantes de todo el mundo trabajar con MPP y C-TAP para hacer que estas tecnologías sean accesibles para las personas que viven en países de bajos y medianos ingresos y ayudar a poner fin a la pandemia
Las 11 tecnologías COVID-19 que se ofrecen bajo dos licencias incluyen la proteína de punta estabilizada utilizada en las vacunas COVID-19 actualmente disponibles, herramientas de investigación para el desarrollo de vacunas, tratamientos y diagnósticos, así como diagnósticos y candidatos a vacunas en etapa inicial.
- Incentivos para participar en C-TAP
Si bien la cantidad de países comprometidos con esta iniciativa es alta, los esfuerzos no han sido suficientes para que esta herramienta extienda su uso a nivel mundial. Por esto, INNOVARTE ONG, en colaboración con LES CHILE y ANDES IP, invitaron a participar en esta encuesta a investigadores, desarrolladores y titulares de tecnologías que están trabajando para combatir el COVID-19 en Latinoamérica para identificar posibles incentivos que autoridades de gobierno y financistas de investigación pudieran implementar a nivel nacional e internacional, con el fin de facilitar la transferencia tecnológica y el licenciamiento no exclusivo de activos de propiedad intelectual relacionados con el COVID -19.
La encuesta fue contestada por centros de investigación, oficinas de transferencia tecnológica, gestores tecnológicos y laboratorios farmacéuticos de varios países de la región: Chile, Ecuador, Perú, Uruguay, Colombia y México.
[1] World Health Organization, COVID-19 Technology Access Pool, https://www.who.int/initiatives/covid-19-technology-access-pool
[2] Organización Mundial de la Salud. Respuesta a la COVID-19. WHA73.1. 19 de mayo de 2020. https://apps.who.int/gb/ebwha/pdf_files/WHA73/A73_R1-sp.pdf
[3] Technology Access Partnership. https://techaccesspartnership.net/
[4] Medicines Patent Pool. https://medicinespatentpool.org/
[5] Open COVID Pledge. https://opencovidpledge.org/
[6] La OMS y el Banco de Patentes de Medicamentos anuncian la primera licencia transparente, mundial y no exclusiva de tecnología contra la COVID-19. https://www.who.int/es/news/item/23-11-2021-who-and-mpp-announce-the-first-transparent-global-non-exclusive-licence-for-a-covid-19-technology
[7] OMS y MPP anuncian acuerdo con NIH para tecnologías sanitarias COVID-19. https://medicinespatentpool-org.translate.goog/news-publications-post/who-and-mpp-announce-agreement-with-nih-for-covid-19-health-technologies?_x_tr_sl=auto&_x_tr_tl=es&_x_tr_hl=auto